Struktur- und Funktionsanalyse / Bildgebung
Radiologie
Die Arbeitsgruppe Experimentelle Radiologie am Institut für Diagnostische Radiologie und Neuroradiologie befasst sich mit der Forschung und Entwicklung neuer bildgebender Verfahren zur Unterstützung einer modernen Diagnostik und Therapie.
Einen Schwerpunkt bildet die klinische und präklinische Magnetresonanztomographie. Im Mittelpunkt stehen dabei die Erprobung, Etablierung und Implementierung neuer Verfahren der Magnetresonanztomographie. Wir unterstützen die interdisziplinäre klinische und präklinische Forschung.
Für die Umsetzung der beschriebenen Ziele stehen folgende Geräte zur Verfügung:
- 1.5 Tesla Avanto Siemens Healthcare, Universitätsmedizin Greifswald
- 1.5 Tesla Aera Siemens Healthcare, Universitätsmedizin Greifswald
- 3.0 Tesla Verio Siemens Healthcare, Universitätsmedizin Greifswald
- 7.1 Tesla ClinScan Bruker, Biotechnikum – Walther Rathenau Strasse 49, Greifswald
Mitglieder:
- Prof. (jr.) Jens-P. Kühn, Arbeitsgruppenleiter
- Stefan Hadlich, Leitender Medizin-Technisch Angestellter
- Katharina Kindermann, Kleintierärztin
Kontakt
Dr. Susan Mouchantat
Universitätsmedizin Greifswald
Institut für Diagnostische Radiologie und Neuroradiologie
Experimentelle Radiologie
E-Mail: susan.mouchantatuni-greifswaldde
Telefon: 03834 86 6914
Die Arbeitsgruppe Funktionelle Bildgebung am Institut für Diagnostische Radiologie und Neuroradiologie befasst sich mit der Erfassung von funktioneller Repräsentation im Gehirn des Menschen. Zudem werden auch Untersuchungen zu strukturellen Gehirnveränderungen in Assoziation mit Krankheit und Lebensführung (SHIP-Studie; Untersuchung des Gehirns) durchgeführt.
Es gibt hierbei folgende Schwerpunkte:
- Emotionsforschung gemeinsam mit dem Institut für Psychologie der Universität Greifswald
- Erforschung der neuronalen Plastizität nach Training und nach Schädigung des Gehirns; Partner vor Ort ist hier vor allem Professor Platz als Chefarzt der BDH-Klinik Greifswald und die Neurologie der Universitätsmedizin Greifswald
- Chronische Schmerzen; Partner vor Ort ist hierbei Professor T. Usichenko aus der Anästhesie der Universitätsmedizin Greifswald
- Temporomandibuläre Schmerzen: Veränderungen der Repräsentation unter erfolgreicher Therapie; Partner ist hierbei Prof. B. Kordaß von der Zahnmedizin Greifswald
Beispielstudie
Kreatives weiterschreiben von Texten im MRT
(Studie gemeinsam mit der Universität Hildesheim und der Neurologie der Universitätsmedizin Greifswald)
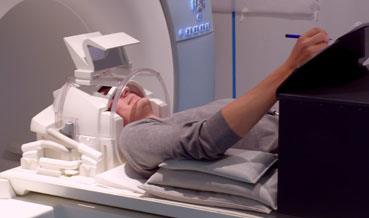
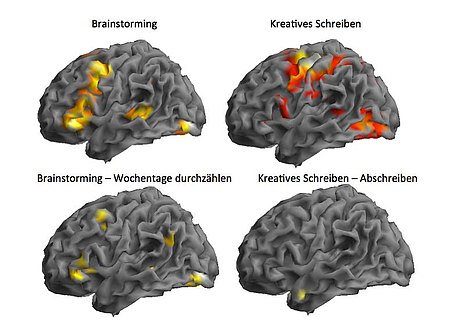
Links
Genauere Informationen zu den Projekten, der laufenden Förderung, den Publikationen, den Mitarbeitern und den methodischen Verfahren finden sich unter folgender Internetseite: www.baltic-imaging-center.de
Kontakt
Prof. Dr. med. Martin Lotze
Universitätsmedizin Greifswald
Institut für Diagnostische Radiologie und Neuroradiologie
Funktionelle Bildgebung
E-Mail: martin.lotzeuni-greifswaldde
Telefon: 03834 86-6899
Mikroskopie und Zytometrie
Die Core Unit (CU) Zytometrie wurde im Jahr 2019 gegründet, und ist in der Abteilung für Immunologie, Institut für Immunologie und Transfusionsmedizin, Universitätsmedizin Greifswald angesiedelt. Das grundlegende Ziel der CU Zytometrie besteht darin, eine Multi-User-Plattform anzubieten, die Wissenschaftler*innen aus allen Einrichtungen der UMG und der Universität Greifswald Zugang zu Spitzentechnologien ermöglicht, und damit die Qualität ihrer Forschung steigert.
Leistungsangebot der CU Zytometrie
1. Durchflusszytometrie
Die Durchflusszytometrie stellt eine leistungsstarke Hochdurchsatztechnologie dar, die zu einem unverzichtbaren Instrument geworden ist, um in kürzester Zeit mehrere Merkmale einzelner Zellen innerhalb einer bestimmten Population zu analysieren. Mit dieser Technologie können Wissenschaftler*innen verschiedene Untersuchungen durchführen, darunter das Expressionsprofil von Oberflächen- und intrazellulären Markern, die Zellzyklusanalyse, die Zellproliferation und den Zelltod (Apoptose oder Nekrose) anstellen.
BD(TM) LSR II ist mit vier Lasern ausgestattet, die bis zu 14 Farben/Parameter gleichzeitig erfassen können. Das BD LSR II verfügt über mehrere wichtige Merkmale, darunter ein fortschrittliches Fluidiksystem, ein einzigartiges optisches System, sowie eine leistungsstarke Datenerfassung und -analyse.
2. Chip-Zytometrie
Neben der Durchflusszytometrie stellt die CU Zytometrie den Anwendenden eine Technologie der nächsten Generation zur Verfügung. Die Chip-Zytometrie ist ein innovatives Werkzeug, das auf der Immobilisierung von Zellen oder Gewebe auf einem speziellen Objektträger ("Chip") basiert. Mit der Chip-Zytometrie können Forschende eine praktisch unbegrenzte Anzahl von Biomarkern von Interesse auf einer einzigen Gewebe- oder Zellsuspensionsprobe analysieren. Der Vorteil der Chip-Zytometrie besteht darin, dass der*die Forscher*in auf Einzelzellniveau arbeiten kann, sowohl in Bezug auf die Morphologie als auch auf die Expressionsprofilierung von Biomarkern (Oberflächen- / intrazellulär). Darüber hinaus können die Chips bis zu zwei Jahre aufbewahrt werden.
Nutzungsgebühren
Die Gebühren für den Betrieb des Durchflusszytometers LSR II richten sich nach den Richtlinien der DFG. Daher hängen die Kosten für die Nutzung der von der CU Zytometrie angebotenen Dienstleistungen von der Art der benötigten Dienstleistung ab.
- Selbstbedienung (Benutzende = Betreibende): 25 € / h
- Betrieb durch Personal der CU Zytometrie oder Schulung durch Personal der CU Zytometrie (CU = Operator): 65 € / h (bis zu 40 h förderbar durch DFG)
Diese Gebühren beinhalten die für den Betrieb der Geräte erforderlichen Grundreagenzien (z.B. sheath fluid t), nicht jedoch spezifische Verbrauchsmaterialien wie Antikörper, Fluorophore oder Zellzählungs-Beads.
Buchung der Instrumente
Registrierte Benutzer*innen können die Instrumente über ein Online-Buchungssystem buchen. Weitere Informationen finden Sie hier.
Wissenschaftliche Kollaborationen und Danksagungen
Alle offiziellen Präsentationen oder Publikationen, die sich aus der Arbeit an der CU Zytometrie ergeben, sollten anerkannt werden. Einige Instrumente wurden aus Zuschüssen oder anderen Quellen erworben, die ebenfalls Anerkennung verdienen. Wir ermutigen auch alle Benutzenden, die Einrichtung in allen wissenschaftlichen Arbeiten anzuerkennen, in denen Forschungsergebnisse veröffentlicht werden, die mit Hilfe der Instrumente der CU Zytometrie generiert wurden.
Core Unit Zytometrie
Abteilung für Immunologie
Sauerbruchstraße, DZ7
3. Etage, Raum J03.07
17475 Greifswald
Kontakt
Dr. VSN Murty Darisipudi, PhD
Wissenschaftlicher Koordinator
Telefon: +49 3834 86-5460/-5465